Die Epigenetik, ein Bereich, der sich mit Veränderungen in der Genexpression befasst, die nicht durch Veränderungen in der DNA-Sequenz bedingt sind, stellt ein dynamisches Feld innerhalb der biologischen Wissenschaften dar. Diese Veränderungen werden durch verschiedene Mechanismen, wie DNA-Methylierung und Histone-Modifikation, herbeigeführt und können durch Umwelteinflüsse, Lebensstil und sogar Ernährung beeinflusst werden. Dieses Wissenschaftsgebiet erweitert unser Verständnis darüber, wie genetische Information tatsächlich zum Ausdruck kommt und welche Faktoren dabei eine Rolle spielen können.
Die Bedeutung der Epigenetik erstreckt sich weit über die akademische Neugier hinaus. Sie hat direkte Auswirkungen auf unser Verständnis von Gesundheit und Krankheit, indem sie mögliche Erklärungen für die Entstehung von Krebs, Herz-Kreislauf-Erkrankungen, neurodegenerativen Störungen und vielem mehr bietet. Zudem wirft sie ein Licht auf die Möglichkeit, dass Lebensstiländerungen und Umweltfaktoren nicht nur unsere eigene genetische Expression beeinflussen können, sondern auch die unserer Nachkommen.
Dieser Artikel zielt darauf ab, ein detailliertes Verständnis der Epigenetik zu vermitteln, von ihren grundlegenden Mechanismen bis hin zu den Auswirkungen auf die menschliche Gesundheit. Dabei wird ein besonderer Fokus auf die Rolle gelegt, die die Epigenetik bei der Entwicklung von Krankheiten spielt, und auf die potenziellen Möglichkeiten, die sie für die Entwicklung neuer therapeutischer Strategien bietet. Durch die Betrachtung aktueller Forschungsergebnisse und die Analyse der Verbindungen zwischen Epigenetik, Umwelt und Lebensstil, strebt der Artikel danach, ein umfassendes Bild dieses aufstrebenden Forschungsfeldes zu zeichnen.
Einführung in die Epigenetik
Definition von Epigenetik
Die Epigenetik befasst sich mit Studien und Phänomenen, die erklären, wie die Aktivität von Genen reguliert und modifiziert werden kann, ohne dass die DNA-Sequenz selbst verändert wird. Diese Modifikationen können die Genexpression an- oder ausschalten und sind entscheidend für viele Prozesse in lebenden Organismen, einschließlich Entwicklung, Zelldifferenzierung und die Anpassung an Umweltbedingungen. Epigenetische Veränderungen sind dynamisch und reversibel, was ihnen eine Schlüsselrolle in der Genregulation zuschreibt.
Abgrenzung von der Genetik
Während die Genetik die Studie der Gene und der Vererbung von Merkmalen von einer Generation zur nächsten ist, fokussiert sich die Epigenetik auf die übergeordneten Mechanismen, die bestimmen, ob und wie diese Gene ausgedrückt werden. Die DNA-Sequenz, die in der Genetik zentral steht, bleibt in der Epigenetik unverändert; stattdessen konzentriert sich das Feld auf die chemischen Modifikationen, die die Zugänglichkeit und Lesbarkeit der DNA beeinflussen, und damit auf die Genexpression einwirken, ohne die Sequenz selbst zu ändern. Diese Lesbarkeit kann von Epigenetik-Tests ermittelt werden.
Grundprinzipien der Epigenetik
Die Epigenetik basiert auf einigen Grundprinzipien, die das Verständnis dieses komplexen Feldes erleichtern:
Reversibilität: Im Gegensatz zu genetischen Mutationen, die dauerhafte Veränderungen in der DNA-Sequenz darstellen, sind epigenetische Modifikationen reversibel. Diese Umkehrbarkeit ermöglicht es Zellen, auf Umweltveränderungen zu reagieren und ihre Genexpression entsprechend anzupassen.
Vererbbarkeit: Bestimmte epigenetische Modifikationen können von einer Generation zur nächsten weitergegeben werden, obwohl sie nicht in der DNA-Sequenz kodiert sind. Dies erweitert das Verständnis von Vererbung über die reine Weitergabe genetischer Information hinaus.
Umwelteinflüsse: Epigenetische Veränderungen können durch Umweltfaktoren wie Ernährung, Stress und Exposition gegenüber Chemikalien induziert werden. Diese Flexibilität ermöglicht es Organismen, ihre Genexpression an veränderte Umweltbedingungen anzupassen.
Zell- und Entwicklungsstadien-spezifische Muster: Epigenetische Modifikationen sind nicht in allen Zellen eines Organismus gleich. Sie variieren zwischen verschiedenen Zelltypen und Entwicklungsstadien, was zur Differenzierung und Spezialisierung von Zellen beiträgt.
Durch die Integration dieser Prinzipien bietet die Epigenetik ein tieferes Verständnis dafür, wie Gene reguliert werden und wie externe Faktoren die Genexpression beeinflussen können, was weitreichende Implikationen für die Gesundheit, Krankheit und die Entwicklung neuer therapeutischer Ansätze hat.
Mechanismen der epigenetischen Regulation
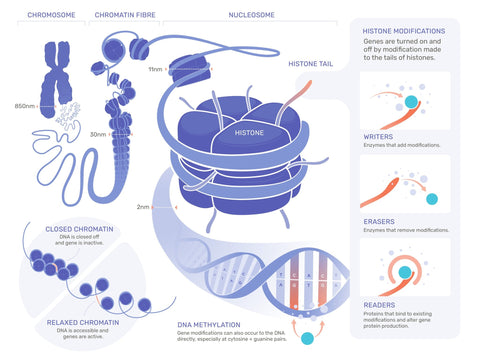
Die Regulation der Genexpression auf epigenetischer Ebene erfolgt hauptsächlich durch drei Mechanismen: DNA-Methylierung, Histone Modifikationen und die Aktivität von nicht-kodierender RNA (ncRNA). Diese Mechanismen wirken zusammen, um die Zugänglichkeit der DNA für Transkriptionsfaktoren zu modifizieren und somit die Genaktivität zu beeinflussen.
DNA-Methylierung
Die Methylierung der DNA ist ein Prozess, bei dem Methylgruppen (CH3) an die Cytosinbasen der DNA angehängt werden, typischerweise an CpG-Dinukleotide. Diese Methylierung wirkt generell genexpressionshemmend. In Regionen mit hoher CpG-Dichte, den sogenannten CpG-Inseln, die oft in Genpromotoren vorkommen, führt eine hohe Methylierungsdichte zur Kompaktierung der DNA und verhindert so die Bindung von Transkriptionsfaktoren und RNA-Polymerase. Dies unterdrückt die Transkription des Gens. Die DNA-Methylierung ist ein entscheidender Mechanismus für die Zelldifferenzierung und die Aufrechterhaltung der Zellidentität.
Histone Modifikationen
Histone sind Proteine, um die sich die DNA wickelt, um die Chromatinstruktur zu bilden. Durch chemische Modifikationen an Histonen, wie Acetylierung, Methylierung, Phosphorylierung und Ubiquitinylierung, kann die Struktur des Chromatins verändert werden, was wiederum die Genexpression beeinflusst. Zum Beispiel führt die Acetylierung von Histon-Tails zur Lockerung der Chromatinstruktur, wodurch die Transkriptionsmaschinerie leichter Zugang zur DNA erhält. Im Gegensatz dazu kann die Methylierung bestimmter Histone die Chromatinstruktur verdichten und die Genexpression hemmen. Diese Modifikationen ermöglichen eine feine Regulation der Genaktivität in Antwort auf zelluläre Signale und Umwelteinflüsse.
Nicht-kodierende RNA (ncRNA)
Nicht-kodierende RNAs sind RNA-Moleküle, die nicht in Proteine übersetzt werden, aber eine wichtige Rolle in der Regulation der Genexpression spielen. Zu den ncRNAs gehören unter anderem Mikro-RNAs (miRNAs) und lange nicht-kodierende RNAs (lncRNAs). miRNAs können an komplementäre Sequenzen in Boten-RNAs (mRNAs) binden und deren Abbau fördern oder die Translation blockieren, was die Proteinproduktion reduziert. LncRNAs sind an einer Vielzahl von regulatorischen Prozessen beteiligt, einschließlich der Chromatinmodifikation, der Genexpression und der Genomstabilität. Durch ihre Fähigkeit, spezifische Gene oder Genregionen zu erkennen und zu binden, spielen ncRNAs eine zentrale Rolle in der epigenetischen Regulation.
Epigenetik, Entwicklung und Alterung
Epigenetische Prägung und Entwicklung
Die epigenetische Prägung ist ein entscheidender Mechanismus, bei dem bestimmte Gene dauerhaft als "an" oder "aus" markiert werden, basierend auf dem Elternteil, von dem sie vererbt wurden. Diese geprägten Gene spielen eine wichtige Rolle in der frühen Entwicklung, da sie die Ausbildung spezifischer Körperstrukturen und -funktionen beeinflussen. Fehlfunktionen in diesem Prozess können zu Entwicklungsstörungen und Krankheiten führen.
Epigenetik in der Embryonalentwicklung
Während der Embryonalentwicklung ermöglichen epigenetische Mechanismen die Differenzierung von Stammzellen zu spezialisierten Zelltypen. Durch das gezielte Ein- und Ausschalten von Genen entstehen aus einer einzigen befruchteten Eizelle die vielfältigen Zelltypen, die für die Bildung eines komplexen Organismus erforderlich sind. Diese Prozesse sind essenziell für die gesunde Entwicklung und das Wachstum.
X-Chromosom-Inaktivierung
Ein weiteres Beispiel epigenetischer Regulation ist die Inaktivierung eines der beiden X-Chromosomen bei weiblichen Säugetieren. Diese Selektion ist zufällig und dient dazu, eine Überexpression der Gene auf dem X-Chromosom zu verhindern. Die Inaktivierung wird durch epigenetische Markierungen gesteuert und ist ein Paradebeispiel für die Bedeutung der Epigenetik in der Entwicklung.
Einfluss der Epigenetik auf die Alterung
Die Epigenetik spielt auch eine entscheidende Rolle im Alterungsprozess. Epigenetische Veränderungen akkumulieren im Laufe des Lebens und können die Funktion von Genen beeinflussen, die für die Aufrechterhaltung der zellulären Integrität und für die Reparaturmechanismen verantwortlich sind. Diese Akkumulation kann zu einer verringerten Fähigkeit der Zellen führen, auf Schäden oder Stressoren zu reagieren, was typische Alterungszeichen und die Entwicklung altersassoziierter Erkrankungen begünstigt.
Vom Standpunkt der Longevity aus betrachtet, bietet die Epigenetik daher einen vielversprechenden Ansatzpunkt, um den Alterungsprozess zu verlangsamen oder umzukehren. Durch gezielte Interventionen, die auf epigenetische Mechanismen abzielen, könnten die Akkumulation schädlicher epigenetischer Veränderungen reduziert und die zelluläre Funktion verbessert werden, was zu einer längeren Gesundheitsspanne und Lebensdauer beitragen könnte.
Einfluss der Umwelt auf die Epigenetik
Die Umwelt spielt eine entscheidende Rolle in der epigenetischen Regulation. Verschiedene externe Faktoren wie Ernährung, Stress und Exposition gegenüber Umweltgiften können signifikante epigenetische Veränderungen hervorrufen, die sich auf die Genexpression und somit auf Gesundheit und Krankheit auswirken können. Dieses Kapitel beleuchtet, wie solche Umwelteinflüsse epigenetische Mechanismen beeinflussen und welche langfristigen Auswirkungen dies haben kann.
Ernährung und Epigenetik
Die Ernährung ist einer der wichtigsten Umweltfaktoren, der epigenetische Veränderungen beeinflussen kann. Bestimmte Nährstoffe und Diäten können die Methylierung der DNA und die Modifikation von Histonen beeinflussen, was wiederum die Genexpression moduliert. Beispielsweise können Folsäure und andere B-Vitamine durch ihre Rolle im Methylierungsprozess die DNA-Methylierungsmuster verändern. Diese Erkenntnisse unterstreichen die Bedeutung einer ausgewogenen Ernährung für die epigenetische Gesundheit und das Potenzial diätetischer Interventionen, um präventiv gegen Krankheiten vorzugehen oder deren Verlauf positiv zu beeinflussen.
Stress und epigenetische Veränderungen
Chronischer Stress kann ebenfalls tiefgreifende Auswirkungen auf das epigenetische Profil eines Individuums haben. Stressbedingte Hormone wie Cortisol können epigenetische Modifikationen in Genen auslösen, die an der Stressantwort und an psychischen Erkrankungen beteiligt sind. Diese Veränderungen können die Reaktion eines Individuums auf zukünftigen Stress beeinflussen und sind mit einem erhöhten Risiko für verschiedene gesundheitliche Probleme, einschließlich Depressionen und Angstzuständen, verbunden. Die Erforschung der epigenetischen Auswirkungen von Stress bietet wichtige Einblicke in die Entstehung dieser Zustände und eröffnet neue Wege für ihre Behandlung.
Umweltgifte und ihre epigenetischen Effekte
Die Exposition gegenüber Umweltgiften wie Schwermetallen, Pestiziden und Luftverschmutzung kann ebenfalls epigenetische Veränderungen hervorrufen. Diese Toxine können die Methylierung der DNA verändern, Histone modifizieren und die Expression von ncRNA beeinflussen, was zu einer dysregulierten Genexpression führt. Solche epigenetischen Veränderungen können zur Entstehung von Krankheiten beitragen und die Vulnerabilität für zukünftige Generationen erhöhen. Die Identifizierung spezifischer epigenetischer Biomarker, die durch Umweltgifte induziert werden, ist von großer Bedeutung, um Expositionsrisiken zu bewerten und präventive Maßnahmen zu entwickeln.
Epigenetik und Krankheiten
Die Erforschung der Epigenetik hat unser Verständnis darüber, wie Krankheiten entstehen und fortschreiten, revolutioniert. Epigenetische Veränderungen sind bei einer Vielzahl von Krankheiten beteiligt, indem sie die Expression von Genen beeinflussen, die für die Aufrechterhaltung der Gesundheit kritisch sind. In diesem Kapitel werden spezifische Beispiele für die Rolle der Epigenetik bei Krebs, neurodegenerativen Erkrankungen und Herz-Kreislauf-Erkrankungen betrachtet.
Krebs und epigenetische Veränderungen
Epigenetische Veränderungen spielen eine zentrale Rolle in der Entstehung und Progression von Krebs. Abnormale DNA-Methylierungsmuster, Histone-Modifikationen und Veränderungen in der Expression von ncRNA können dazu führen, dass Tumorsuppressorgene unterdrückt und Onkogene aktiviert werden. Diese Dysregulation begünstigt Zellwachstum und -teilung außer Kontrolle und trägt zur Krebsentwicklung bei. Die Identifizierung epigenetischer Marker bei verschiedenen Krebsarten eröffnet neue Möglichkeiten für die Früherkennung, Prognose und Entwicklung zielgerichteter Therapien, die spezifisch epigenetische Abnormalitäten adressieren.
Epigenetik bei neurodegenerativen Erkrankungen
Auch bei neurodegenerativen Erkrankungen wie Alzheimer, Parkinson und Huntington spielen epigenetische Mechanismen eine wichtige Rolle. Epigenetische Modifikationen können die Expression von Genen beeinflussen, die für die neuronale Funktion und Plastizität wichtig sind, und dadurch zur Pathologie dieser Erkrankungen beitragen. Beispielsweise kann eine veränderte Methylierung der DNA zu einer reduzierten Expression neuroprotektiver Gene führen, was den neurodegenerativen Prozess beschleunigt. Forschungen in diesem Bereich zielen darauf ab, epigenetische Biomarker zu identifizieren, die als Frühwarnsysteme für neurodegenerative Erkrankungen dienen könnten, sowie therapeutische Ansätze zu entwickeln, die auf die Wiederherstellung normaler epigenetischer Muster abzielen.
Herz-Kreislauf-Erkrankungen und Epigenetik
Die Epigenetik beeinflusst auch die Entstehung und Progression von Herz-Kreislauf-Erkrankungen. Epigenetische Veränderungen können durch Faktoren wie Ernährung, Rauchen und körperliche Aktivität induziert werden und sich auf Gene auswirken, die an der Regulierung des Blutdrucks, der Cholesterinspiegel und der Entzündungsreaktion beteiligt sind. Diese genetischen Modifikationen können zur Entwicklung von Atherosklerose, Herzinfarkt und Schlaganfall beitragen. Die Untersuchung epigenetischer Mechanismen in diesem Kontext bietet wertvolle Einblicke in die Prävention und Behandlung von Herz-Kreislauf-Erkrankungen, indem sie aufzeigt, wie Lebensstiländerungen zu einer Verbesserung der epigenetischen Gesundheit führen können.
Epigenetik: Ein Wegweiser für Gesundheit und Langlebigkeit
Die Epigenetik eröffnet uns einzigartige Perspektiven auf die Zusammenhänge zwischen unseren Lebensgewohnheiten und der Gesundheit auf zellulärer Ebene. Anstatt sich auf die Behandlung von Krankheiten zu konzentrieren, wenn sie bereits entstanden sind, unterstreicht die epigenetische Forschung die Bedeutung der Prävention und der proaktiven Erhaltung der Gesundheit. Durch das Verständnis, wie bestimmte Lebensstilfaktoren unsere Gene beeinflussen, können wir gezieltere Strategien entwickeln, um das Wohlbefinden zu fördern und den Alterungsprozess positiv zu beeinflussen.
Bewegung und epigenetische Effekte
Regelmäßige körperliche Aktivität hat nachweislich positive Auswirkungen auf die epigenetische Regulation. Bewegung kann die Methylierungsmuster der DNA in einer Weise verändern, die zur Aktivierung von Genen beiträgt, die die Zellreparatur und die Verlängerung der Telomere unterstützen. Diese Veränderungen können die biologische Alterung verlangsamen und das Risiko für altersbedingte Erkrankungen verringern.
Die Rolle der Ernährung und Nahrungsergänzung
Die Ernährung spielt eine entscheidende Rolle bei der Modulation epigenetischer Marker. Lebensmittel und Nährstoffe, die reich an Folsäure, Betain, Vitamin B12 und anderen methylierungsfördernden Komponenten sind, können die DNA-Methylierung unterstützen und damit zu einer gesunden Genexpression beitragen. Nahrungsergänzungsmittel wie NAD+ Booster wirken sich direkt auf die Sirtuin-Pfade aus, die eine zentrale Rolle in den Longevity Pathways spielen, und können somit potenziell die Lebensdauer verlängern und die Gesundheit verbessern.
Stressmanagement und seine epigenetischen Auswirkungen
Chronischer Stress kann negative epigenetische Veränderungen hervorrufen, die mit einer Vielzahl von Gesundheitsproblemen in Verbindung gebracht werden. Strategien zur Stressreduktion, wie Meditation, Yoga und andere Entspannungstechniken, können helfen, diese epigenetischen Effekte zu minimieren und das allgemeine Wohlbefinden zu verbessern.
Lebensstilfaktoren: Schlaf und Umwelt
Ausreichender und qualitativ hochwertiger Schlaf ist entscheidend für die epigenetische Gesundheit. Schlafmangel kann zu ungünstigen Methylierungsmustern führen, die mit einem erhöhten Risiko für verschiedene Krankheiten verbunden sind. Ebenso kann die Reduzierung der Exposition gegenüber schädlichen Umweltgiften epigenetische Schäden minimieren und die Gesundheit fördern.
Epigenetik im Alltag: Prävention, Vererbung und personalisierte Medizin
Die fortschreitende Entschlüsselung epigenetischer Mechanismen bietet nicht nur Einblicke in die biologischen Grundlagen von Gesundheit und Krankheit, sondern eröffnet auch neue Möglichkeiten, wie wir diese Erkenntnisse im Alltag umsetzen können. Von der Beeinflussung der epigenetischen Vererbung bis hin zur Entwicklung personalisierter medizinischer Ansätze, die auf den individuellen epigenetischen Profilen basieren, steht uns eine Revolution in der Gesundheitsvorsorge bevor.
Lebensstil und epigenetische Vererbung
Aktuelle Forschungen zeigen, dass unsere Lebensstilentscheidungen nicht nur unsere eigene Gesundheit beeinflussen, sondern auch epigenetische Markierungen hinterlassen können, die an zukünftige Generationen weitergegeben werden. Dieses Phänomen, bekannt als epigenetische Vererbung, bedeutet, dass die Effekte unserer Ernährung, unseres Stresslevels und unserer Umweltexpositionen möglicherweise über unsere eigene Lebensspanne hinausreichen. Diese Erkenntnis unterstreicht die Bedeutung eines gesunden Lebensstils nicht nur für unser eigenes Wohlergehen, sondern auch als Vermächtnis für unsere Nachkommen.
Präventive Maßnahmen und epigenetische Diagnostik
Die Integration epigenetischer Biomarker in präventive Screening-Programme könnte die Früherkennung und Prävention von Krankheiten revolutionieren. Durch die Identifizierung von Individuen mit einem hohen Risiko für bestimmte Krankheiten können gezielte präventive Maßnahmen ergriffen werden, lange bevor die ersten Symptome auftreten. Epigenetische Diagnostik bietet das Potenzial, individuell zugeschnittene Empfehlungen für Ernährung, Bewegung und Stressmanagement zu liefern, um die Gesundheit zu optimieren und das Krankheitsrisiko zu minimieren.
Zukunft der personalisierten Medizin durch Epigenetik
Die personalisierte Medizin, die auf den individuellen genetischen und epigenetischen Profilen der Patienten basiert, steht an der Schwelle zu einem Durchbruch. Die epigenetische Forschung trägt dazu bei, Behandlungsstrategien zu entwickeln, die speziell auf die einzigartigen epigenetischen Muster jedes Einzelnen abgestimmt sind. Dieser Ansatz verspricht nicht nur eine effektivere Behandlung von Krankheiten, sondern auch die Minimierung von Nebenwirkungen und die Maximierung der Therapieerfolge. In Zukunft könnte die epigenetische Analyse ein Standardinstrument in der medizinischen Praxis werden, um maßgeschneiderte Gesundheitspläne zu erstellen, die auf die individuellen Bedürfnisse und Risikoprofile der Patienten zugeschnitten sind.
Abschluss und Ausblick
Die Reise durch die Welt der Epigenetik hat uns ein tiefes Verständnis dafür vermittelt, wie Umweltfaktoren, Lebensstil und Ernährung unsere Genexpression beeinflussen und dadurch unsere Gesundheit und unser Wohlbefinden prägen. Von der Prägung in der embryonalen Entwicklung bis hin zur epigenetischen Vererbung und den personalisierten Therapien hat die Epigenetik unser Wissen über die Dynamik von Gesundheit und Krankheit revolutioniert.
Bedeutung von Epigenetik
Die Epigenetik überbrückt die Lücke zwischen Genetik und Umwelteinflüssen und bietet damit ein komplexes Bild davon, wie Gene und Lebensstil zusammenwirken. Diese Erkenntnisse haben nicht nur unser Verständnis von Vererbung und Genexpression erweitert, sondern auch gezeigt, wie modifizierbar und anpassungsfähig unser biologisches System tatsächlich ist. Die Möglichkeit, durch gezielte Interventionen in epigenetische Prozesse einzugreifen, eröffnet neue Wege in der Prävention, Diagnostik und Therapie von Krankheiten.
Aktuelle Forschungstrends
Die aktuelle Forschung konzentriert sich zunehmend auf die Entschlüsselung spezifischer epigenetischer Muster, die mit bestimmten Krankheitsbildern assoziiert sind, und die Entwicklung von Technologien zur gezielten Modifikation dieser Muster. Ein besonderes Augenmerk liegt auf der Identifizierung epigenetischer Biomarker, die für die Früherkennung von Krankheiten genutzt werden können, und auf der Erforschung von Substanzen, die gezielt epigenetische Veränderungen herbeiführen oder rückgängig machen können.
Potenzial für zukünftige Entdeckungen
Die Zukunft der epigenetischen Forschung verspricht spannende Entwicklungen, insbesondere im Bereich der personalisierten Medizin. Die Möglichkeit, individuelle epigenetische Profile zu nutzen, um präzise und maßgeschneiderte Behandlungspläne zu erstellen, könnte die Effektivität therapeutischer Interventionen erheblich verbessern. Darüber hinaus könnten Fortschritte in der Epigenetik dazu beitragen, die Mechanismen der Alterung besser zu verstehen und Ansätze zu entwickeln, die eine gesunde Langlebigkeit fördern.
Mit jedem Schritt, den die epigenetische Forschung voranschreitet, erweitern wir unser Verständnis davon, wie wir Gesundheit nicht nur erhalten, sondern auch aktiv gestalten können. Die Epigenetik steht im Zentrum einer neuen Ära der Biomedizin, in der präventive und personalisierte Ansätze an Bedeutung gewinnen. Indem wir das immense Potenzial der Epigenetik weiter erforschen und nutzen, öffnen sich uns neue Möglichkeiten, das menschliche Wohlbefinden zu fördern und die Herausforderungen zu bewältigen, die uns auf dem Weg zu einer gesünderen und längeren Lebensspanne begegnen.